고려대학교 교수소개
Knowledge & Innovation
소개

Prof. 박해철
Tel: 031-412-6713
E-mail: hcpark67@korea.ac.kr
- Profile
- Curriculum Vitae
- Publication
- Research
- Lab Members
Profile
Affiliation
Department of Biomedical Sciences, Korea University
Address
Dept. of Biomedical Sciences, Korea University Ansan Hospital 516 Gojan1-dong, Danwon-gu, Ansan-si Gyeonggi-do, South Korea 425-707
Curriculum Vitae
Education
- 1985 ~ 1993 B.S. in Genetic Engineering, Kyungpook National University
- 1993 ~ 1995 M.S. in Genetic Engineering, Kyungpook National University
- 1995 ~ 2000 Ph.D. in Genetic Engineering, Kyungpook National University
Employment
- 2000 ~ 2005 Research Associate, Dept. of Biological Sciences, Vanderbilt University, USA
- 2005 ~ 2006 Research Assistant Professor, Dept. of Biological Sciences, Vanderbilt University, USA
- 2006 ~ 2009 Assistant Professor, Graduate school of Medicine, Korea University
- 2009 ~ 2013 Associate Professor, Graduate school of Medicine, Korea University
- 2013 ~ at present Professor, Department of Biomedical Sciences, Korea University
Publication
Publication
- Kim E, Jeong I, Chung AY, Kim S, Kwon SH, Seong JY, Park HC. "Distribution and neuronal circuit of spexin 1/2 neurons in the zebrafish CNS." (2019). Sci Rep. doi: 10.1038/s41598-019-41431-7.
- Rah YC, Han EJ, Park S, Rhee J, Koun S, Park HC, Choi J. “In vivo assay of the potential gadolinium-induced toxicity for sensory hair cells using a zebrafish animal model” (2018). J. Appl. Toxicol. doi: 10.1002/jat.3656.
- Jeong I, Kim E, Kim S, Kim HK, Lee DW, Seong JY, Park HC. “mRNA expression and metabolic regulation of npy and agrp1/2 in the zebrafish brain” (2018). Neuroscience Letters. 668:73-79.
- Rah YC, Yoo MH, Choi J, Park S, Park HC, Oh KH, Lee SH, Kwon SY. "In vivo assessment of hair cell damage and developmental toxicity caused by gestational caffeine exposure using zebrafish (Danio rerio) models" (2017). Neurotoxicol Teratol. 64, 1-7.
- Lee S, Elvitigala DAS, Lee S, Kim HC, Park HC, Lee J. “Molecular characterization of a bactericidal permeability-increasing protein/lipopolysaccharide-binding protein from black rockfish (Sebastes schlegelii): Deciphering its putative antibacterial role” (2017). Dev Comp Immunol. 67:266-275.
- Jo M, Chung AY, Yachie N, Seo M, Jeon H, Nam Y, Seo Y, Kim E, Zhong Q, Vidal M, Park HC*, Roth FP*, Suk K*. “Yeast genetic interaction screen of human genes associated with amyotrophic lateral sclerosis: identification of MAP2K5 kinase as a potential drug target” (2017). Genome Research 27,1487-1500. (*Corresponding author)
- Jang HW, Chun SH, Park HC, Ryu HJ, Kim IH. “Comparative study of dual-pulsed 1064 nm Q-switched Nd:YAG laser and single-pulsed 1064 nm Q-switched Nd:YAG laser by using zebrafish model and prospective split-face analysis of facial melasma” (2017). J Cosmet Laser Ther. 19(2):114-123.
- Choi H, Shin JH, Kim ES, Park SJ, Bae IH, Jo YK, Jeong IY, Kim HJ, Lee Y, Park HC, Jeon HB, Kim KW, Lee TR, Cho DH. Primary Cilia Negatively Regulate Melanogenesis in Melanocytes and Pigmentation in a Human Skin Model. (2016) PLoS One. 12;11(12)
- Bathige SD, Umasuthan N, Jayasinghe JD, Godahewa GI, Park HC*, Lee J*. “Three novel C1q domain containing proteins from the disk abalone Haliotis discus discus: Genomic organization and analysis of the transcriptional changes in response to bacterial pathogens.” (2016). Fish Shellfish Immunol. pii:S1050-4648(16)30432-6.(*Corresponding author)
- Ryu HJ, Lee JM, Jang HW, Park HC, Rhyu IJ, Kim IH. Morphologic Changes of Zebrafish Melanophore after Intense Pulsed Light and Q-Switched Nd:YAG Laser Irradiation. (2016). Ann Dermatol. 28(6):711-717.
- Kim KT, Kim N, Kim HK, Lee H, Gruner HN, Gergics P, Park C, Mastick GS, Park HC, Song MR. "ISL1-based LIM complexes control Slit2 transcription in developing cranial motor neurons" (2016). Scientific Reports 6,36491.
- Kim E, Jeong I, Kim S, Kim HK, Lee DW, Kim B, Seong JY, Bae YK, Ryu JH, Park HC. “Distribution of galanin receptor 2b neurons and interaction with galanin in the zebrafish central nervous system.” (2016). Neuroscience Letters. 628:153-60.
- Bathige SD, Umasuthan N, Park HC*, Lee J*. “An invertebrate signal transducer and activator of transcription 5(STAT5) ortholog from the disk abalone, Haliotis discus discus: Genomic structure, early developmental expression, and immune responses to bacterial and viral stresses.” (2016) Dev Comp Immunol. 56, 46-56. (*Corresponding author)
- Chang J, Choi J, Rah YC, Yoo MH, Oh KH, Im GJ, Lee SH, Kwon SY, Park HC, Chae SW, Jung HH. "Sodium Selenite Acts as an Otoprotectant against Neomycin-Induced Hair Cell Damage in a Zebrafish Model" (2016). PLoS One 11(3):e0151557. doi: 10.1371/journal.
- Yoo MH, Rah YC, Choi J, Park S, Park HC, Oh KH, Lee SH, Kwon SY. “Embryotoxicity and hair cell toxicity of silver nanoparticles in zebrafish embryos” (2016). Int J Pediatr Otorhinolaryngol.83:168-74.
- Thulasitha WS, Umasuthan N, Jayasooriya RG, Noh JK, Park HC*, Lee J*. “A thioredoxin domain-containing protein 12 from black rockfish Sebastes schlegelii: Responses to immune challenges and protection from apoptosis against oxidative stress” (2016) Comp Biochem Physiol C Toxicol Pharmacol. 185-186, 29-37. (*Corresponding author)
- Rah YC, Choi J, Yoo MH, Yum G, Park S, Oh KH, Lee SH, Kwon SY, Cho SH, Kim S, Park HC. “Ecabet sodium alleviates neomycin-induced hair cell damage” (2015) Free Radic Biol Med. 89:1176-83.
- Lee SK, Oh KH, Chung AY, Park HC, Lee SH, Kwon SY, Choi J. “Protective role of quercetin against cisplatin-induced hair cell damage in zebrafish embryos” (2015). Hum Exp Toxicol. 34(11):1043-52.
- Kim S, Lee YI, Chang KY, Lee DW, Cho SC, Ha YW, Na JE, Rhyu IJ, Park SC, Park HC. “Promotion of Remyelination by Sulfasalazine in a Transgenic Zebrafish Model of Demyelination” (2015). Mol. Cells. 38(11),1013-1021.
- Elvitigala DA, Whang I, Nam BH, Park HC*, Lee J* “Identification of a myeloperoxidase-like ortholog from rock bream (Oplegnathus fasciatus), deciphering its transcriptional responses to induced pathogen stress” (2015) Fish Shellfish Immunology 45(2), 477-485 (*Corresponding author)
- Yoo MG, So BJ, Lee JM, Kim do H, Park HC, Ryu HJ, Kim IH. “Influence of Pulse Type on Subcellular Selective Photothermolysis of Melanosomes in Adult Zebrafish Skin Following 1,064-nm, Q-switched, Nd:YAG Laser Irradiation: A Pilot Study” (2015). Ann Dermatol. 27(2):230-2.
- Paik H, Chung AY, Park HC, Park RW, Suk K, Kim J, Kim H, Lee K, Butte AJ. "Repurpose terbutaline sulfate for amyotrophic lateral sclerosis using electronic medical records" (2015) Scientific Reports doi: 10.1038/srep08580.
- Choi J, Chang J, Jun HJ, Im GJ, Chae SW, Lee SH, Kwon SY, Jung HH, Chung AY, Park HC. "Protective role of edaravone against neomycin-induced ototoxicity in zebrafish" (2014) Journal of Applied Toxicology 34(5), 554-561.
- Kim HY, Yang DH, Shin SW, Kim MY, Yoon JH, Kim S, Park HC, Kang DW, Min D, Hur MW, Choi KY. "CXXC5 is a transcriptional activator of Flk-1 and mediates bone morphogenic protein-induced endothelial cell differentiation and vessel formation" (2014) FASEB J. 28(2), 615-626.
- Song JJ, Chang J, Choi J, Im GJ, Chae SW, Lee SH, Kwon SY, Jung HH, Chung AY, Park HC, Choi J. “Protective role of NecroX-5 against neomycin-induced hair cell damage in zebrafish” (2014) Archievs of Toxicology 88(2), 435-441
- Park MK, Im GJ, Chang J, Chae SW, Yoo J, Han WG, Hwang GH, Jung JY, Choi J, Jung HH, Chung AY, Park HC, Choi J. “Protective effects of caffeic acid phenethyl ester (CAPE) against neomycin-induced hair cell damage in zebrafish” (2014). Int J Pediatr Otorhinolaryngol. 78(8):1311-5.
- Chung AY, Kim S, Kim E, Kim D, Jeong I, Cha YR, Bae YK, Park SW, Lee J, Park HC. “Indian hedgehog B function is required for the specification of oligodendrocyte progenitor cells in the zebrafish CNS” (2014). Journal of Neuroscience 33(4), 1728-1733.
- Chung AY, Kim PS, Kim S, Kim E, Kim D, Jeong I, Kim HK, Ryu JH, Kim CH, Choi J, Seo JH, Park HC. “Generation of demyelination models by targeted ablation of oligodendrocytes in the zebrafish CNS” (2014). Molecules and Cells 36, 82-87.
- Song JJ, Chang J, Choi J, Im GJ, Chae SW, Lee SH, Kwon SY, Jung HH, Chung AY, Park HC, Choi J. “Protective role of NecroX-5 against neomycin-induced hair cell damage in zebrafish” (2014) Archievs of Toxicology 88(2), 435-441
- Park MK, Im GJ, Chang J, Chae SW, Yoo J, Han WG, Hwang GH, Jung JY, Choi J, Jung HH, Chung AY, Park HC, Choi J. “Protective effects of caffeic acid phenethyl ester (CAPE) against neomycin-induced hair cell damage in zebrafish” (2014). Int J Pediatr Otorhinolaryngol. 78(8):1311-5.
- Chang J, Im GJ, Chae SW, Lee SH, Kwon SY, Jung HH, Chung AY, Park HC, Choi J. "Protective Role of Trimetazidine Against Neomycin-induced Hair Cell Damage in Zebrafish" (2013) Clin. Exp. Otorhinolarygol. 6(4), 219-225.
- Chung AY, Kim PS, Kim S, Kim E, Kim D, Jeong I, Kim HK, Ryu JH, Kim CH, Choi J, Seo JH, Park HC. “Generation of demyelination models by targeted ablation of oligodendrocytes in the zebrafish CNS” (2013). Molecules and Cells 36, 82-87.
- Hong SJ, Im GJ, Chang J, Chae SW, Lee SH, Kwon SY, Jung HH, Chung AY, Park HC, Choi J. “Protective effects of edaravone against cisplatin-induced hair cell damage in zebrafish” (2013). Int J Pediatr Otorhinolaryngol. 77(6), 1025-1031.
- Kim KH, Park HJ, Kim JH, Kim S, Williams DR, Kim MK, Jung YD, Teraoka H, Park HC, Choy HE, Shin BA, Choi SY. “Cyp1a reporter zebrafish reveals target tissues for dioxin” (2013). Aquatic Toxicology. 134-135, 57-65.
- Chung AY, Kim S, Kim E, Kim D, Jeong I, Cha YR, Bae YK, Park SW, Lee J, Park HC. “Indian hedgehog B function is required for the specification of oligodendrocyte progenitor cells in the zebrafish CNS” (2013). Journal of Neuroscience 33(4), 1728-1733.
- Jung IH, Leem GL, Jung DE, Kim MH, Kim EY, Kim SH, Park HC, Park SW. “Glioma is formed by active Akt1 alone and promoted by active Rac1 in transgenic zebrafish” (2013). Neuro-oncology 15(3), 290-304.
- Bathige SD, Whang I, Umasuthan N, Lim BS, Park MA, Kim E, Park HC*, Lee J*. "Interferon regulatory factors 4 and 8 in rock bream, Oplegnathus fasciatus: structural and expressional evidence for their antimicrobial role in teleosts" (2012). Fish Shellfish Immunology 33(4), 857-871. (*Corresponding author)
- Kim S, Kim JD, Chung AY, Kim HS, Kim YS, Kim MJ, Koun SI, Lee YM, Rhee M, Huh, TL, Park HC. "Antagonistic regulation of PAF1C and pTEF-b is required for oligodendrocyte differentiation" (2012). Journal of Neuroscience 32, 8201-8207.
- Umasuthan N, Bathige SD, Revathy KS, Lee Y, Whang I, Choi CY, Park HC*, Lee J*. "A manganese superoxide dismutase (MnSOD) from Ruditapes philippinarum: comparative structural- and expressional-analysis with copper/zinc superoxide dismutase (Cu/ZnSOD) and biochemical analysis of its antioxidant activities" (2012). Fish Shellfish Immunology 33(4), 753-765. (*Corresponding author)
- Kim JH, Kim DH, Kim JH, Lee SG, Kim HS, Park HC, Kim IH. "Recovery of Pigmentation Following Selective Photothermolysis in Adult Zebrafish Skin: Clinical Implications for Laser Toning Treatment of Melasma" (2012). Journal of Cosmetic and Laser Therapy. Oct 11. (Epub ahead of print).
- Premachandra HK, Whang I, Lee YD, Lee S, De Zoysa M, Oh MJ, Jung SJ, Lim BS, Noh JK, Park HC*, Lee J*. "Cystatin B homolog from rock bream Oplegnathus fasciatus: genomic characterization, transcriptional profiling and protease-inhibitory activity of recombinant protein" (2012). Comp Biochem Physiol B Biochem Mol Biol. 163(1), 138-146.
- Kim JH, Kim DH, Kim JH, Lee SG, Kim HS, Park HC, Kim IH. Elvitigala DA, Whang I, Premachandra HK, Umasuthan N, Oh MJ, Jung SJ, Yeo SY, Lim BS, Lee JH, Park HC*, Lee J*. "Caspase 3 from rock bream (Oplegnathus fasciatus): genomic characterization and transcriptional profiling upon bacterial and viral inductions" (2012). Fish Shellfish Immunology. 33(1):99-110. (*Corresponding author)
- Saranya Revathy K, Umasuthan N, Whang I, Lee Y, Lee S, Oh MJ, Jung SJ, Choi CY, Park CJ, Park HC*, Lee J*. "A novel acute phase reactant, serum amyloid A-like 1, from Oplegnathus fasciatus: Genomic and molecular characterization and transcriptional expression analysis" (2012). Developmental and Comparative Immunology. 37(2):294-305. (*Corresponding author)
- Choi J, Im GJ, Chang J, Chae SW, Lee SH, Kwon SY, Chung AY, Park HC, Jung HH. "Protective effects of apocynin on cisplatin-induced ototoxicity in an auditory cell line and in zebrafish" (2011). Journal of Applied Toxicology Kim S, Chung AY, Kim D, Kim YS, Kim HS, Kwon HW, Huh TL, Park HC. “Tcf3 function is required for the inhibition of oligodendroglial fate specification in the spinal cord of zebrafish embryos” (2011). Molecules and Cells 32, 383-388.
- Ahn HJ, Park Y, Kim S, Park HC, Seo SK, Yeo SY, Geum D. “The expression profile and function of Satb2 in zebrafish embryonic development” (2010). Molecules and Cells 30, 377-382.
- Chung AY, Kim MJ, Kim D, Bang S, Hwang SW, Lim CS, Lee S, Park HC*, Huh TL*. "Neuron-specific expression of atp6v0c2 in zebrafish CNS." (2010). Developmental Dynamics 239, 2501-2508. (*Corresponding author)
- Kim JH, Kim H, Park HC, Kim IH. (2010). "Subcellular Selective Photothermolysis of Melanosomes in Adult Zebrafish Skin Following 1064-nm Q-Switched Nd:YAG Laser Irradiation" Journal of Investigative Dermatology 130, 2333-2335.
- Nam DH, Oh JS, Nam MH, Park HC, Lim CS, Lee WJ, Sattabongkot J, Klein TA, Ayala FJ. (2010). "Emergence of new alleles of the MSP-3alpha gene in Plasmodium vivax isolates from Korea" American Journal of Tropical Medicine and Hygiene 82, 522-524.
- Hwang J, Lee S, Lee JT, Kwon TK, Kim DR, Kim H, Park HC, Suk K. (2010). "Gangliosides induce autophagic cell death in astrocytes" British Journal of Pharmacology 159, 586-603.
- Jung SH, Kim S, Chung AY, Kim HT, So JH, Ryu J, Park HC*, Kim CH*. (2010). “Visualization of myelination in GFP-transgenic zebrafish” Developmental Dynamics 239, 592-597. (*Corresponding author)
- Bae SY*, Park HC*, Oh JS, Yoon SY, Park DW, Choi IK, Kim HJ, Oh JH, Hur DS, Chung C, Chang JK, Robinson JP, Lim CS. (2009). “Absolute CD4+ cell count using a plastic microchip and a microscopic cell counter” Cytometry Part B-Clinical Cytometry 76, 345-353. (*Equal contribution)
- Son SW, Kim JH, Kim SH, Kim H, Chung AY, Choo JB, Oh CH, Park HC. (2009). “Intravital imaging in zebrafish using quantum dots” Skin Research and Technology. 15, 157-160.
- Lee S, Park JY, Lee WH, Kim H, Park HC, Mori K, Suk K. (2009). "Lipocalin-2 is an autocrine mediator of reactive astrocytosis" The Journal of Neuroscience 29, 234-249.
- Kim HT, Kim EH, Yoo KW, Lee MS, Choi JH, Park HC, Yeo SY, Lee DS, Kim CH. (2008). "Isolation and expression analysis of Alzheimer's disease-related gene xb51 in zebrafish" Developmental Dynamics 237, 3921-3926.
- Kim H, Kim S, Chung AY, Bae YK, Hibi M, Lim CS, Park HC. (2008). “Notch-regulated perineurium development from zebrafish spinal cord” Neuroscience Letters 448, 240-244.
- Hwang J, Zheng LT, Ock J, Lee MG, Kim SH, Lee HW, Lee WH, Park HC, Suk K. (2008). "Inhibition of glial inflammatory activation and neurotoxicity by tricyclic antidepressants" Neuropharmacology 55, 826-834.
- Kim SH, Nam MH, Roh KH, Park HC, Nam DH, Park GH, Han ET, Klein TA, Lim CS. (2008). "Evaluation of a rapid diagnostic test specific for Plasmodium vivax" Tropical Medicine & International Health 13, 1495-1500.
- Kim S, Kim SH, Kim H, Chung AY, Cha YI, Kim CH, Huh TL, Park HC. (2008). “Frizzled 8a function is required for oligodendrocyte development in the zebrafish spinal cord” Developmental Dynamics 237, 3324-3331.
- Kim H, Shin J, Kim S, Poling J, Park HC*, Appel B. (2008). “Notch-regulated oligodendrocyte specification from radial glia in the spinal cord of zebrafish embryos” Developmental Dynamics 237, 2081-2089. (*Corresponding author)
- Kucenas, S., Takada, N., Park, H.C., Woodruff, E., Broadie, K., Appel, B. (2008). " CNS-derived glia ensheath peripheral nerves and mediate motor root development" Nature Neuroscience 11, 143-151
- Park, H. C., Shin, J., Roberts, R. K., Appel, B. (2007). "An olig2 reporter gene marks oligodendrocyte precursors in the postembryonic spinal cord of zebrafish." Developmental Dynamics 236, 3402-3407.
- Shin, J., Poling, J., Park, H.C., Appel, B. (2007). "Notch signaling regulates neural precursor allocation and binary neuronal fate decisions in zebrafish" Development 134, 1911-1920.
- Won, M., Ro, H., Park, H.C., Kim, K.E., Huh, T.L., Kim, C.H. and Rhee, M. (2006). "Dynamic expression patterns of zebrafish 1G5 (1G5z), a calmodulin kinase-like gene in the developing nervous system" Developmental. Dynamics 235, 835-842.
- Park, H. C., Boyce, J., Shin, J. and Appel, B. (2005). "Oligodendrocyte specification in zebrafish requires notch-regulated cyclin-dependent kinase inhibitor function" Journal of Neuroscience 25, 6836-6844
- Park, H. C., Shin, J., Appel B. (2004). "Spatial and temporal regulation of ventral spinal cord precursor specification by Hedgehog signaling." Development 131, 5959-5969
- Shin, J*., Park, H. C*., Topczewska, J. M., Mawdsley, D. J., Appel, B. (2003). "Neural cell fate analysis in zebrafish using olig2 BAC transgenics." Methods in Cell Science 25, 7-14. (* Equal contribution) Park, H. C., Appel, B. (2003) "Delta-Notch signaling regulates oligodendrocyte specification." Development 130, 3747-3755.
- Yoo, K. W., Kim, C. H., Park, H. C., Kim, S. H., Kim, H. S., Hong, S. K., Han, S., Rhee, M., Huh, T. L. (2003). "Characterization and expression of a presomitic mesoderm-specific mespo gene in zebrafish." Development Genes and Evolution 213, 203-206.
- Kim, S.H., Shin, J., Park H. C., Yeo, S. Y., Hong, S. K., Han, S., Rhee, M., Kim, C. H., Chitnis, A. B., Huh,T. L. (2002). "Specification of an anterior neuroectoderm patterning by Frizzled8a-mediated Wnt8b signalling during late gastrulation in zebrafish." Development 129, 4443-4455.
- Park, H.-C.,Mehta, A., Richardson, J.S. and Appel, B. (2002). "olig2 is required for zebrafish primary motor neuron and oligodendrocyte development" Developmental Biology 248, 56-368.
- Park, H.-C., Kim, C.-H., Bae, Y.-K., Hong, S.-K., Yeo, S-Y. Hibi, M. and Hirano, T. and Huh, T.-L. (2000). "Analysis of Upstream Elements in the HuC Promoter Leads to the Establishment of Transgenic Zebrafish with Fluorescent Neurons" Developmental Biology 227, 279-293.
Patents
- 1. 이용현, 허태린, 박진서, 박해철, 재조합 미생물을 이용한 폴리-베타-하이드록시부탄산의 제조방법, 특허 제120802호, 특허번호10-120802-0000, 대한민국, 1997년 8월 21일 (등록)
- 2. 이용현, 허태린, 박진서, 박해철, 폴리(3-하이드록시부티릭산-3-하이드록시발레릭산)과 폴리(3-하이드록시부티릭산-4-하이드록시부티릭산)의 제조방법, 특허 제159905호, 특허번호 10-159905-0000, 대한민국, 1998년 8월 13일 (등록)
- 3. 허태린, 박해철, 김철희, 김형석 신경특이적 유전자 발현을 조절하는 제브라피쉬의 HuC프로모터 유전자, 이를 이용한 형광성신경을 갖는 형질전환 동물 및 그의 제조방법, 그리고 이를 이용한 신경변이체 동물의 선별방법, 특허 제0429397호, 대한민국, 2004년 4월 16일 (등록)
- 4. Huh, T. L., Park, H. C., Kim, C. H. and Kim, H. S. Zebrafish HuC promoter capable of directing neuron-specific expression of structural genes, transgenic animal having HuC promoter and its generation, and method for screening neuronal mutant animals using the transgenic animal, PCT/KR01/01259, 2001. 7. 24.; WO 02/18594 A1, 2002. 3. 7. 미국출원번호 : 10/296,6652002. 11. 25 공개번호:US 2004/0093630 A1 (출원)
- 5. 동물의 시각 인식을 이용한 생리활성 물질의 스크리닝 장치 및 방법, 특허번호 10-1365732/3, 대한민국, 2014년 2월14일 (등록)
- 6. 어류의 선천적 색상 선호 행동을 이용한 아세틸콜린 관련 생리 활성 물질의 탐색 방법, 특허번호 10-1443738/3, 대한민국, 2014년 9월 17일 (등록)
- 7. 프로테인 포스파타아제 저해제 2의 신규용도, 특허번호 10-1473153/4, 대한민국, 2014년 12월 9일
- 8. 어류의 시각 인식을 이용한 생리 활성 물질의 스크리닝 용 수용 부재 및 이를 포함하는 장치, 특허번호 10-1479204/3, 대한민국, 2014년 12월 29일 (등록)
- 9. MEK5 또는 PEX2 활성 억제제를 유효성분으로 포함하는 퇴행성 신경질환 예방 및 치료용 약학적 조성물 및 이를 스크리닝하는 방법, 특허번호 10-1755032/3, 대한민국, 2017년 6월 30일(등록)
Research
Research Topic
Zebrafish는 신경계에 특이적으로 형광을 발현하는 transgenic fish를 이용하면 신경세포의 형성 및 이동이나 분화 과정을 생체 내에서 쉽게 관찰할 수 있으므로 기존의 척추동물 모델들이 가지고 있는 신경계연구의 여러 가지 문제점들을 극복하게 해주어 신경계의 발생 및 분화 과정 연구에 많이 사용되고 있습니다. 따라서 본 연구실에서는 각종 신경계 특이적 형광발현 transgenic zebrafish 및 돌연변이체들을 이용하여 척추동물 신경계의 발생 및 분화과정과 성체 신경계 줄기세포의 분화조절기작에 대하여 연구를 진행하고 있으며, 또한 다양한 신경계 질환동물모델을 제조하여 이들의 발생기전 규명 및 치료물질 탐색을 위한 연구를 수행하고 있습니다.
1. 희소돌기아교세포 분화 및 수초화 기작 연구
희소돌기아교세포(oligodendrocyte)는 중추신경계 내에서 수초(myelin)를 생성하여 신경세포의 축삭을 감싸고 있음으로써 축삭을 주위로부터 절연시켜 전기적 신호전달 속도를 높여주며, 주변 환경에 대해서 보호해주는 역할을 수행하고 있는 신경교세포(glia)입니다 (그림 1). 따라서 신경세포가 정상적으로 작동하기 위해서는 수초화에 의한 신경세포와 희소돌기아교세포의 정확한 신경네트워크 형성이 필수적으로 요구됩니다. 이러한 수초화(myelination)는 손상을 받으면 탈수초화(demyelination)가 진행이 되고, 정상적인 경우에는 다시 희소돌기아교세포 전구체에 의하여 손상된 부위에 새로운 수초형성-재수초화(remyelination)-가 이루어지는 것으로 알려져 있습니다. 그러나 노화, 독성물질, 유전요인 및 자가면역질환 등 다양한 원인에 의해 재수초화 조절기전에 문제가 생기면 새로운 수초 형성이 이루어지지 않게 되며, 따라서 신경세포에서 원활한 전기신호전달이 이루어지지 않아 발생부위에 따라 운동마비, 언어장애 등의 증상이 나타나는 탈수초화 질환의 증상이 보이게 됩니다. 가장 대표적인 탈수초화 질환 중 하나인 다발성경화증(mutiple sclerosis)는 전 세계에 약 250만명의 환자가 존재하는 가장 흔한 중추신경계 질환이지만, 현재까지 사용되는 치료제들은 대부분 자가면역작용을 조절하는 약물이며, 아직까지 재수초화을 유발하여 증상을 회복시킬 수 있는 치료제는 개발되어 있지 않습니다. 따라서 다양한 탈수초화 질환 환자에서 재수초화를 유도하여 증상을 회복시킬 수 있는 근본적인 치료제의 개발이 필요하며, 이를 위해 생체 내에서 희소돌기아교세포의 생성 및 분화, 그리고 수초화 조절기전에 대한 연구가 필요합니다.
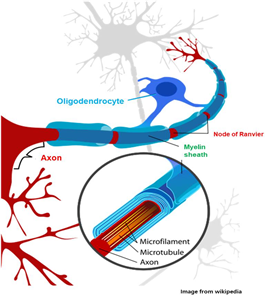
>그림1. 신경세포의 축삭을 감싸고 있는 희소돌기아교세포의 수초
수초화 조절 기전 연구는 수초와 신경세포의 축삭과의 상호작용을 연구해야하며 따라서 세포주를 이용한 in vitro 시스템으로는 연구가 어렵습니다. 따라서 본 연구실에서는 희소돌기아교세포의 분화 및 수초화를 생체 내에서 관찰할 수 있는 zebrafish 동물모델 (그림 2) 이용하여 oligodendrocyte의 분화조절기작을 밝힘으로써 다발성경화증의 정확한 발생 원인을 규명하고자 노력하고 있습니다.

>그림 2. 형질전환 제브라피쉬를 이용한 희소돌기아교세포와 수초의 이미징
1) Neural stem cells and adult oligodendrogenesis
희소돌기아교세포는 발생과정 뿐 아니라 성체에서도 계속적으로 생성되고 있으나 성체에서 회소돌기아교세포를 생성하는 줄기세포의 규명 및 이들의 분화조절기전 연구는 많이 이루어지지 않고 있습니다. 따라서 본 연구실에서는 확보된 각종 희소돌기아교세포 특이적 형광발현 형질전환 제브라피쉬 및 신경줄기세포 특이적 형광발현 제브라피쉬들을 이용하여 먼저 성체의 뇌에 분포하는 모든 희소돌기아교세포 생성 줄기세포(olig2+ 방사교세포)들의 위치를 확인(그림 3)하고 이들의 줄기세포로서의 특성을 규명하고 있습니다. 또한 형질전환 제브라피쉬를 이용하여 시공간적으로 희소돌기아교세포의 세포사멸을 유도하고 그들의 재생기작을 연구하고 있습니다.

> 그림 3. 제브라피쉬 성체의 전뇌에서 희소돌기아교세포 생성 줄기 세포의 탐색
2) Demyelination model and screening for remyelination factor
본 연구실에서는 먼저 생체 내에서 탈수초화를 유도하기 위하여 분화된 희소돌기아교세포에서 특이적으로 발현하는 mbp 유전자의 promoter와 Gal4-UAS transactivator system을 이용하여 분화된 희소돌기아교세포 특이적으로 nfsB 독성유전자를 발현시키는 mbp:Gal4/uas:nfsB-mCherry transgenic 제브라피쉬를 제조하였습니다 (그림 4). 현재는 제조된 탈수초화 동물모델을 이용하여 재수초화를 촉진시키는 신규 약물 및 유전자 screening하고 그들의 기능 연구를 진행하고 있습니다.

>그림 4. Gal4-UAS transactivator system을 이용한 희소돌기아교세포 특이적 nfsB-mCherry 세포독성유전자 발현 transgenic zebrafish
3) Motor nerve and schwann cell myelination
슈반세포(Schwann cell)는 말초신경계를 구성하는 운동신경의 축삭에 수초를 형성하여 전기적 신호전달 속도를 높여 자극에 대한 즉각적인 운동반응을 유도하는 신경교세포(glia)입니다. 이뿐만 아니라 운동신경의 정상적인 축삭 성장과 재생 그리고 근육과의 신경연접에 중요한 역할을 담당하기 때문에 두 세포사이의 상호작용은 중요합니다. 그래서 본 연구실에서는 운동신경과 슈반세포를 실시간으로 관찰이 가능한 제브라피쉬 형질전환모델을 이용해(그림 5) 운동신경의 발생과 슈반세포의 분화 그리고 수초화 작용기전에 대한 연구를 수행하고 있고, 나아가 퇴행성 운동신경계 질환연구로 영역을 확장하고 있습니다.
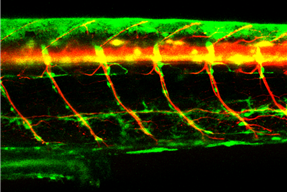
>그림 5. 형질전환 제브라피쉬를 이용한 운동신경과 슈반세포 이미징
2. 근위축성 축색경화증 (Amyotrophic lateral sclerosis, 루게릭병) 연구
근위축성측색경화증(ALS)은 루게릭병으로 불리는 대표적인 운동신경원 질환(motor neuron disease, MND)으로써 뇌와 척수에 존재하는 운동신경세포에 선택적으로 퇴행성 변화가 생겨 근육 쇠약 및 위축을 유발하고 결국엔 사망에 이르는 치명적인 퇴행성 신경계 질환입니다. 그러나 현재까지 ALS를 유발하는 정확한 원인에 대해서는 밝혀지지 않았으며, ALS 질환을 완치할 수 있는 근본적인 치료제는 개발되어 있지 않습니다. 본 연구실에서는 운동신경세포 및 축삭돌기(axon)와 축삭돌기를 감싸고 있는 희소돌기아교세포 및 수초(myelin) 특이적으로 형광단백질을 발현하는 제브라피쉬 형질전환모델을 활용하여 생체 내 이미징 및 제브라피쉬 행동 분석을 기반으로 하여 ALS 질환 연구를 진행하고 있습니다. ALS 환자에서 밝혀져 있는 ALS 원인 유전자를 대상으로 병리기전을 규명하기 위해 제브라피쉬 운동신경세포 및 희소돌기아교세포 특이적으로 ALS 원인 유전자를 발현시킨 후 운동신경세포 및 축삭돌기와 수초의 퇴화 과정을 연구하고 있습니다. 또한 현재까지 알려져 있지 않은 ALS 질환 관련 유전자를 발굴하는 연구와 함께 치료제 탐색 시스템 구축을 위한 연구를 수행하고 있습니다.

>그림 1. 제브라피쉬에서 사람의 ALS 질환 유전자로 알려져 있는 SOD1 변이 유전자 발현을 통한 ALS 질환 유발 검증. 정상적인 제 브라피쉬와 비교하여 SOD1 변이 유전자를 발현시킨 제브라피쉬에서 운동신경세포의 축삭돌기(적색형광단백질) 퇴화 및 수 초(녹색형광단백질)의 퇴화가 관찰되었음.
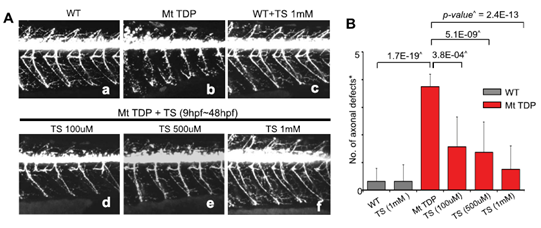
>그림 2. 제브라피쉬 모델을 이용한 ALS 치료제 탐색. 사람의 ALS 질환 유전자로 알려져 있는 TDP-43를 발현시킨 제브라피쉬에서 turbutaline sulfate(TS) 약물의 효과 검증. (Paik H et al., Sci Rep. 2015)
3. 신경펩타이드(Neuropeptide) 기능 연구
신경펩타이드(Neuropeptide)는 신경조절물질의 하나로 신경세포에서 합성 및 분비되어 정보를 전달하고 이를 통해 섭식, 대사, 생식, 수면, 감정, 사회적 행동 등 뇌의 다양한 생리 활성 기능을 조절합니다. 신경펩타이드의 발현 이상은 다양한 신경계 질환을 유발하는 원인이 되며, 따라서 신경펩타이드 및 수용체는 관련 질환의 약물개발을 위한 주요한 표적인자로서 연구되고 있습니다. 신경펩타이드의 기능 및 조절기전에 관한 연구는 오래전부터 꾸준히 이루어지고 있지만, 여전히 아직 기능이 알려지지 않은 신경펩타이드와 그 수용체가 많이 존재하며 이들이 어떻게 뇌의 생리적 기능을 조절하는지 많이 알려져 있지 않습니다. 본 연구실에서는 공동 연구를 통하여 인간의 신규 신경펩타이드와 높은 상동성을 가진 제브라피쉬 신규 신경펩타이드를 발굴 및 동정하였습니다. 발굴된 신규 신경펩타이드의 특이적인 형광 형질전환 제브라피쉬를 제조하여 신규 신경펩타이드의 신경회로(Neural circuit)를 분석하고 신경펩타이드 과발현 형질전환 제브라피쉬 및 기능소실(knockout) 제브라피쉬를 제조하여 이들을 이용한 다양한 행동 연구를 수행하고 있습니다. 이를 통하여, 생체 내에서 신규 신경펩타이드의 신경회로가 어떻게 구성되어있고, 이러한 신경회로를 통하여 신경펩타이드가 중추신경계에서 어떠한 생리적 기능을 수행하는지 규명하는 연구를 수행하고 있습니다.

>그림 1.제브라피쉬 중추신경계에서 신규 신경펩타이드1(적색형광)과 신규 신경펩타이드2(녹색형광)의 발현패턴
4. 치아 발생 (Tooth development) 연구
치아는 입속/ 인두(제브라피쉬)에 돌출되어 있어 저작 작용을 하는 신체 기관이며 말을 할 때 발음에 있어서도 역할을 하기 때문에 의사소통에도 상당히 중요합니다. 치아의 수와 형태에 있어서의 대부분의 이상은 유치(젖니)보다 영구치에서 더 빈번히 관찰되며, 특히 치아가 상실되었을 때 임플란트를 통한 기능적인 수복은 가능하나 치주인대와 감각신경의 부재와 같은 한계를 갖기 때문에 자연적인 치아를 재생시키기 위한 연구가 필요합니다. 치아 교체가 일어나지 않는 동물모델 쥐와는 달리, 제브라피쉬는 새로운 치아의 발생을 통한 교체가 일생동안 계속 이루어지므로 사람의 영구치 형성에 관련된 기전에 대한 동물모델로 적합합니다. 본 연구실에서는 치아세포 특이적 형광 형질전환 제브라피쉬를 이용하여 기본적인 치아발생 분만 아니라 어떻게 새로운 치아가 형성되고 교체가 이루어지는지를 관찰하고, 각종 유도 형질전환 제브라피쉬 시스템과 신호 차단/ 활성 약물들을 이용하여 Notch 또는 Wnt signaling을 조절하는 방법을 통하여 새로운 치아 형성과정에서의 신호전달체계를 규명하는 연구를 수행하고 있습니다.
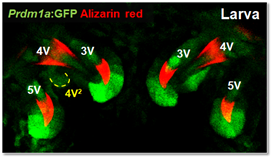
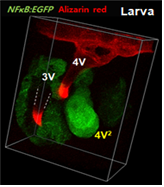
>그림 1. 제브라피쉬 larva에서 발생중인 치아(녹생형광)의 이미징. 첫 번째 치아 (4V)의 발생이 끝나 전반적으로 무기질 (적색형광)이 확인되며, 이의 교체치아인 (4V2)의 발생이 확인됨.
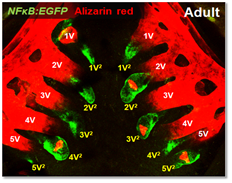
>그림 2. 제브라피쉬 성체에서 기존의 치아(적색형광)와 이를 교체할 새롭게 발생중인 치아(녹색형광)의 이미징
Lab Members

Suhyun Kim(Ph.D.)

Eunmi Kim(Ph.D.)
E-mail : dieslunae@naver.com E-mail : kemsj@hanmail.net Research field
: Oligodendrocyte development and myelination. / ALSResearch field
: Neuropeptide. / ALS
Inyoung Jeong(Ph.D.)

Hwan-Ki Kim(graduate student)
E-mail : inyoung1096@naver.com E-mail : zelkovae@nate.com Research field
: Neuropeptide.
Research field
: Neural stem cells and adult oligodendrogenesis.
Dong-Won Lee(graduate student)

BoA Kim(graduate student)
E-mail : ldw0920@hanmail.net E-mail : queenbee31@naver.com Research field
: Motor nerve and schwann cell myelination.Research field
: Tooth development
Yongbo Seo(graduate student)

Eun Jung Han(graduate student)
E-mail : ybs4428@naver.com E-mail : hoj7843@naver.com Research field
: Neural stem cells.Research field
: Vestibular disease.
